La autofagia es el proceso por el que tus células se comen a sí mismas. Suena mal. Es bueno. Es el sistema de reciclaje más sofisticado que existe en biología, y cuando funciona bien, elimina proteínas dañadas, orgánulos viejos y patógenos intracelulares que de otro modo se acumularían y acelerarían el envejecimiento.
El problema es que desde que Yoshinori Ohsumi ganó el Nobel de Fisiología o Medicina en 2016, la palabra entró en el vocabulario wellness y con ella llegaron las fantasías: actívala a las 12 horas de ayuno, el café la dispara, la curcumina la multiplica por 10. Ninguna de esas afirmaciones es exacta. Esta es la versión real.
Qué es la autofagia (y para qué sirve realmente)
Autofagia viene del griego autos (uno mismo) y phagein (comer). Es un proceso conservado evolutivamente que existe en levaduras, gusanos, ratones y humanos. Su función principal es el control de calidad intracelular: degrada y recicla componentes celulares dañados para que la célula pueda reutilizar sus bloques fundamentales.
Hay tres tipos principales:
- Macroautofagia: la más estudiada. La célula forma una doble membrana (fagóforo) que engloba el material a degradar y lo fusiona con un lisosoma. Esto es lo que la mayoría llama "autofagia".
- Microautofagia: el lisosoma invagina directamente y captura material citoplasmático.
- Autofagia mediada por chaperonas (CMA): selectiva para proteínas con una secuencia específica (KFERQ). Muy relevante en neuronas.
¿Para qué sirve en términos prácticos? La autofagia limpia agregados proteicos (relacionados con Alzheimer y Parkinson), elimina mitocondrias disfuncionales (mitofagia), destruye bacterias y virus intracelulares, y recicla aminoácidos en períodos de ayuno. Un nivel basal de autofagia es esencial para la supervivencia celular. El problema no es "poca autofagia" sino un desequilibrio crónico entre acumulación de daño y capacidad de limpieza.
Siempre hay un nivel basal de autofagia activa. Lo que puedes hacer es aumentar su flujo de forma significativa. La diferencia entre "autofagia encendida" y "autofagia aumentada" es crucial para entender qué esperar.
El Nobel de Ohsumi: lo que descubrió realmente
Yoshinori Ohsumi, trabajando en la Universidad de Tokio y más tarde en el Instituto Tecnológico de Tokio, usó levaduras de panadería (Saccharomyces cerevisiae) para identificar los genes responsables de la autofagia. En 1993 publicó el primer mapa de genes ATG (autophagy-related genes). En 2016, la Academia Sueca le premió con el Nobel "por sus descubrimientos de los mecanismos de autofagia".
Lo que descubrió: al privar de nutrientes a levaduras con vacuolas transparentes (equivalentes al lisosoma en mamíferos), las vacuolas se llenaban rápidamente de vesículas. Identificó 15 genes ATG esenciales. Muchos de ellos tienen homólogos directos en humanos. Este trabajo fue la base para entender cómo las células "deciden" degradar sus propios componentes y cuándo.
La relevancia para la longevidad viene de estudios posteriores que conectaron la autofagia deficiente con acumulación de proteínas tóxicas en enfermedades neurodegenerativas, y la autofagia activa con extensión de vida en modelos animales.
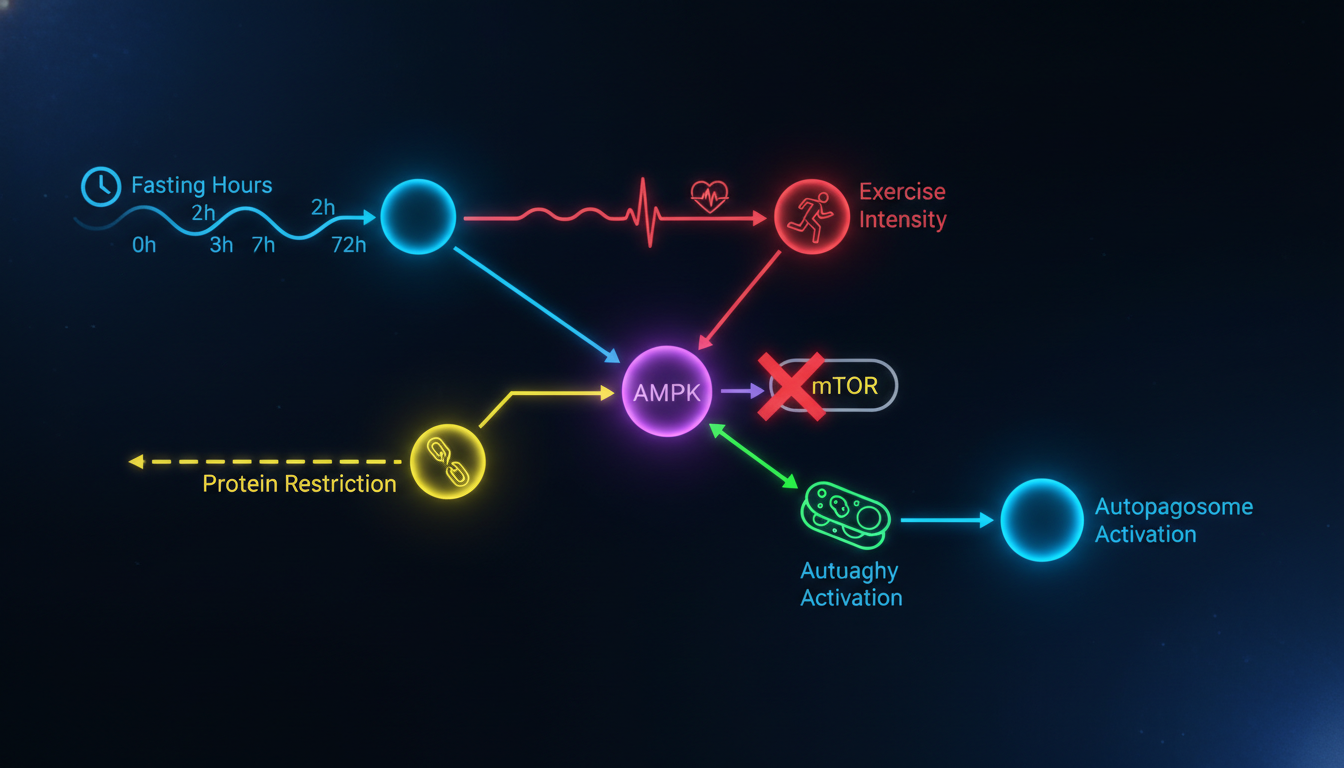
Los interruptores moleculares: mTOR, AMPK y ULK1
La autofagia no se activa ni se inhibe de forma simple. Hay dos sensores energéticos principales que actúan como reguladores opuestos:
mTORC1: el inhibidor maestro
mTOR (mechanistic Target Of Rapamycin, Complejo 1) es el freno de la autofagia. Cuando hay abundancia de nutrientes —especialmente aminoácidos ramificados (leucina), glucosa e insulina alta— mTORC1 está activo y fosforila (inhibe) ULK1, el iniciador de la autofagia. Mientras comas, mTOR está activo y la autofagia está suprimida. Esto es fisiológicamente correcto: no tiene sentido reciclar componentes cuando hay energía abundante.
AMPK: el sensor de escasez
AMPK (AMP-activated Protein Kinase) es el sensor de energía baja. Cuando la relación AMP/ATP sube (menos energía disponible), AMPK se activa y hace dos cosas: inhibe mTORC1 y activa directamente ULK1. Resultado: autofagia encendida. AMPK se activa con ayuno, ejercicio de resistencia, restricción calórica y también con metformina.
ULK1: el iniciador
ULK1 (Unc-51-like kinase 1) es la proteína que inicia la formación del fagóforo cuando mTOR lo deja de inhibir. Es el punto de convergencia de las señales. Sin ULK1 activo, no hay autofagia.
| Condición | mTORC1 | AMPK | Autofagia |
|---|---|---|---|
| Fed state (comida abundante) | ↑ Activo | ↓ Inactivo | Baja |
| Ayuno >12-14h | ↓ Inhibido | ↑ Activo | Aumentando |
| Ejercicio intenso | ↓ Inhibido (post) | ↑ Muy activo | Alta (intra-ejercicio) |
| Restricción proteica | ↓ Moderado | Variable | Moderada-alta |
Cómo activar la autofagia: los inductores con evidencia real
1. Ayuno: el inductor más potente
El ayuno es la forma más eficaz, directa y gratuita de aumentar la autofagia. Al dejar de ingerir calorías, la insulina cae, mTOR se inhibe y AMPK sube. La autofagia empieza a aumentar de forma medible, en estudios en humanos con biopsias musculares, entre las 18 y las 24 horas de ayuno.
El mito de "las 12 horas" viene de extrapolaciones de estudios en ratón. En ratones el metabolismo es 7 veces más rápido, así que sus "12 horas" equivalen aproximadamente a 3-4 días humanos en términos de señalización metabólica. En humanos, un estudio de 2010 publicado en Autophagy (Mizushima et al.) mostró que la autofagia en músculo esquelético humano aumenta significativamente después de 24-48 horas de ayuno, no a las 12.
Eso no significa que el 16/8 no sirva: sirve para mantener un tono autofágico basal elevado comparado con quien come 5 veces al día. Pero si quieres autofagia seria, los ayunos de 24-72h ocasionales son mucho más potentes.
2. Restricción calórica sostenida
Una restricción calórica del 20-30% sin llegar al ayuno también activa AMPK de forma crónica y mantiene mTOR en un tono más bajo. No es tan potente como el ayuno agudo, pero el efecto acumulado durante meses puede ser superior en términos de extensión de vida, al menos en modelos animales. Los estudios CALERIE en humanos sugieren mejoras en marcadores de autofagia con restricción del 25% durante 2 años.
3. Restricción proteica selectiva
mTOR es especialmente sensible a los aminoácidos, en particular a la leucina. Reducir la ingesta de leucina (presente en altas concentraciones en carne, whey, lácteos) inhibe mTOR incluso sin restricción calórica total. Esto explica por qué las dietas plant-based con proteína moderada se asocian a menor actividad mTOR. La restricción proteica al 0.8 g/kg de peso (frente a los 1.6-2g habituales en entrenadores) parece activar rutas autofágicas, aunque hay un trade-off con la masa muscular que no se puede ignorar.
Ejercicio y autofagia: el efecto que más se subestima
El ejercicio es probablemente el segundo inductor más potente de autofagia después del ayuno, y el más subestimado en la literatura popular. Durante el ejercicio de resistencia aeróbica, la autofagia se activa en músculo esquelético, hígado y corazón. El mecanismo principal es AMPK: el ejercicio sube la relación AMP/ATP dramáticamente.
Un estudio clave de He et al. publicado en Nature en 2012 demostró que ratones con una mutación que impedía la autofagia inducida por ejercicio no obtenían los beneficios metabólicos del entrenamiento (mejora de glucosa, reducción de grasa). Esto sugiere que parte de los beneficios del ejercicio están mediados por la autofagia.
El tipo de ejercicio importa:
- Cardio Zona 2 (60-70% FC máx, 45-90 min): activa AMPK de forma sostenida. Probablemente el más autofágico por tiempo de ejercicio.
- HIIT y sprint: activa AMPK de forma aguda e intensa, pero por períodos más cortos.
- Fuerza: activa autofagia durante y post, pero también activa mTOR en la fase de recuperación (necesario para la síntesis proteica y reparación).
Polifenoles: resveratrol, espermidina y quercetina
Esta es la zona de más hype y más matices. Los polifenoles pueden activar autofagia a través de varias rutas, pero la evidencia en humanos es mucho más débil que en cultivos celulares o ratones.
Espermidina: el más prometedor
La espermidina es una poliamina presente en el trigo germinado, soja fermentada (natto), champiñones y queso curado. Activa autofagia inhibiendo EP300 (acetiltransferasa que inhibe proteínas autofágicas). Un estudio observacional de Kiechl et al. (2018, American Journal of Clinical Nutrition) mostró que alta ingesta dietética de espermidina se asoció a menor mortalidad cardiovascular en una cohorte austriaca de 829 participantes seguidos 20 años. La dosis fue de ~80-90 µmol/día. Atención: es observacional, no causal.
Suplementos: 1-2 mg/día de espermidina (trigo germinado concentrado) son los rangos usados en ensayos piloto. Frank Madeo, investigador en Graz, lidera los ensayos clínicos más relevantes actualmente.
Resveratrol: promesa incumplida
El resveratrol activa SIRT1 (sirtuina 1), que tiene conexión indirecta con la autofagia. Sin embargo, las dosis en estudios con resultados en ratón son 100-200 mg/kg (imposibles de trasladar a humanos) y los ensayos clínicos humanos han sido mayoritariamente decepcionantes. David Sinclair (Harvard) lleva años popularizando el resveratrol; la comunidad científica más crítica, incluyendo Charles Brenner, señala que los mecanismos SIRT1 en humanos no replican los efectos de restricción calórica.
Si tomas resveratrol: 150-500 mg/día, con grasa para absorción. Expectativas bajas.
Quercetina: doble función
La quercetina activa autofagia, pero también tiene actividad senolítica (elimina células senescentes). Presente en manzanas, cebolla roja y alcaparras. En cultivos celulares activa autofagia a 10-50 µM, concentraciones difíciles de alcanzar con dieta sola. Como suplemento: 500-1000 mg/día. Tiene buena biodisponibilidad con pimienta negra (piperina).
Curcumina
Activa autofagia en estudios in vitro principalmente. La biodisponibilidad oral de la curcumina simple es muy baja (<1%). Con fosfolípidos (Meriva) o nanopartículas se mejora. El hype es desproporcionado respecto a la evidencia en humanos.
Cuándo NO conviene activar autofagia
Aquí está el punto que el mundo wellness omite completamente: la autofagia excesiva es tan problemática como la deficiente.
Cáncer en estadío activo
Las células tumorales pueden usar la autofagia como mecanismo de supervivencia bajo el estrés de la quimioterapia. En algunos tipos de cáncer, activar autofagia puede proteger a las células tumorales. Esta es un área activa de investigación —algunos oncólogos están estudiando inhibidores de autofagia (como la cloroquina) como adyuvantes— pero la dirección no está clara. Si tienes cáncer activo, no experimentes con ayunos prolongados sin supervisión oncológica.
Después de entrenamiento de fuerza
Si quieres masa muscular, inhibir mTOR (activar autofagia) justo después del entrenamiento es contraproducente. La síntesis proteica muscular requiere mTOR activo. Por eso la ventana post-entreno es el peor momento para ayunar agresivamente: necesitas aminoácidos y mTOR activado para crecer.
Déficit calórico severo con poco músculo
En personas con sarcopenia o muy bajo porcentaje muscular, forzar autofagia con ayunos prolongados puede provocar catabolismo muscular neto. La autofagia degrada también proteínas musculares. Primero construye base muscular, luego juega con ayunos.
Embarazo y lactancia
Ayunos prolongados no están indicados durante el embarazo. El feto tiene sus propios requisitos de señalización mTOR para crecer. No experimentes.
Preguntas frecuentes
¿El café activa la autofagia?
El café contiene cafeína, que puede activar levemente AMPK, y ácido clorogénico, con actividad antioxidante. Hay algún estudio en ratón mostrando que el café (incluyendo descafeinado) aumentó marcadores de autofagia en hígado. En humanos no hay evidencia directa sólida. Lo que sí hace el café es no romper el ayuno si lo tomas solo (sin leche ni azúcar), así que prolonga el período de mTOR bajo.
¿Cuánto tiempo de ayuno necesito para "activar" autofagia útil?
Para autofagia basal elevada: 14-16 horas son suficientes para mantener mTOR en tono bajo. Para autofagia robusta y medible: 24-48 horas. Para efectos máximos (regeneración de células madre): 72 horas o más, y aquí ya hablamos de protocolos que requieren preparación y, en muchos casos, supervisión médica.
¿El ayuno intermitente 16/8 diario da más autofagia que un ayuno de 48h semanal?
No necesariamente. Un ayuno de 48h semanal activa la autofagia de forma mucho más intensa que 7 ayunos de 16h. La profundidad importa más que la frecuencia para efectos autofágicos agudos. Para beneficios metabólicos generales (insulina, triglicéridos), el 16/8 diario es más consistente.
¿La rapamicina activa autofagia?
Sí: la rapamicina inhibe directamente mTORC1 y activa la autofagia. Es el fármaco más estudiado para extensión de vida en mamíferos (múltiples estudios del National Institute on Aging). Sin embargo, también inmunosuprime y tiene efectos secundarios significativos. Uso off-label en longevidad a dosis bajas (1-6 mg semanal, no diario) está siendo investigado, pero no es algo para tomar sin médico especializado.
Autofagia real = ayuno >18h con regularidad + ejercicio aeróbico (Zona 2) + ingesta de espermidina dietética (trigo germinado, natto, champiñones) + control de leucina si no estás en fase de ganancia muscular. No pagues suplementos caros esperando milagros que el ayuno consigue gratis.